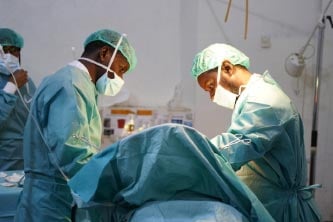
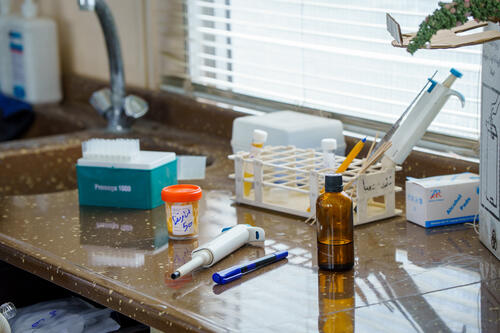
Discover all our latest news, stories and publications. Use the filter to get to the content you're looking for.

MSF contrainte de réduire ses activités humanitaires médicales à Kabo

MSF forced to reduce medical activities in Kabo
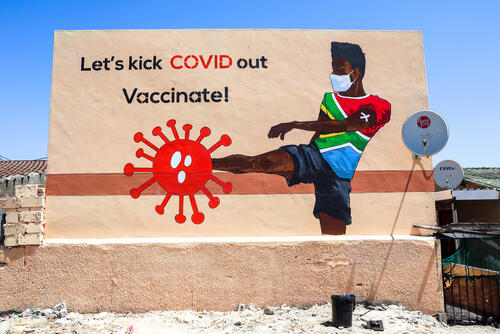
Vaccinating people with comorbidities in South Africa
Processos de qualificação de MSF para produtos médicos
Tal como muitos outros atores humanitários, MSF é consciente de que a qualidade dos medicamentos e outros produtos médicos nem sempre é devidamente garantida no mercado global (Road map for access to medicines, vaccines and other health products 2019-2023, WHO). A coordenação de Garatia de Qualidade (GQ) da IO (Escritório internacional) desenvolveu os 3 Esquemas de Qualificação para a aprovação interna de
- medicamentos,
- dispositivos médicos (MD), diagnóstico in vitro (IVD), artigos de laboratório e
- alimentos médicos especializados (SF) para serem utilizados nos seus programas.
Princípios
- A qualificação é um procedimento padronizado de avaliação da qualidade para validar (ou não) os produtos médicos antes de poderem ser comprados para uso por MSF, verificando se o produto cumpre pelo menos as normas de qualidade reconhecidas internacionalmente. O processo de qualificação consiste na avaliação de um dossier de produto e de um local de fabricação (por exemplo, auditoria BPF).
- Os procedimentos de qualificação de MSF são baseados na confiança mútua. Pede-se ao fabricante que certifique a veracidade e exatidão das informações e documentos enviados a MSF. Erros ou omissões podem levar à desqualificação do produto e/ou do fabricante.
- Os esquemas de qualificação de MSF não se destinam a interferir com a iniciativa de pré-qualificação da OMS, nem a duplicar qualquer trabalho existente conduzido por rigorosas Autoridades Reguladoras Nacionais. Assim, MSF conta com o Programa de Pré Qualificação da OMS (PQ) e do registo em países altamente regulamentados, quando aplicável.
- MSF não é uma Agência Reguladora / organismo de certificação. O Esquema de Qualificação de MSF foi concebido exclusivamente para a organização e as decisões tomadas só são válidas para MSF. As decisões são tomadas utilizando um sistema de classificação pré-definido, para assegurar a imparcialidade.
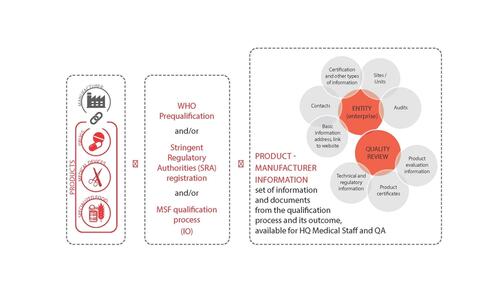
Abordagem
As diferentes etapas do processo são baseadas no seguinte:
- Avaliação baseada em questionário(s) do produto e/ou do fabricante
- Avaliação de BPF do local de fabricação
- Acompanhamento e seguimento ativo
MSF Qualification Schemes

Processo de qualificação de medicamentos de MSF

Processo de qualificação de MSF para dispositivos medicais e diagnósticos in vitro
Processo de qualificação de MSF para alimentos para fins medicinais especiais
Se a avaliação for bem sucedida, é emitida uma "Ficha de Especificação do Produto" (PSS) que resume as características do produto tal como aprovado pelo MSF, e é utilizada como referência para as compras.
A qualificação MSF é um procedimento contínuo e os produtos aprovados são monitorizados a intervalos regulares. As atividades de monitorização centram-se na reavaliação da conformidade com as BPF do local de fabricação e na atualização das informações e dados fornecidos na avaliação do produto.
Expressão de interesse
Os fabricantes/fornecedores de produtos médicos (medicamentos, vacinas, produtos alimentares especializados, reagentes e equipamento laboratorial, material e equipamento médico) são bem-vindos para manifestar o seu interesse em tornar-se um fornecedor validado por MSF, enviando um e-mail para o assistente dos coordenadores de GQ [email protected]
Produtos não incluídos na lista de MSF de Medicamentos, lista de MSF de Alimentos Especializados ou lista de MSF de Dispositivos Médicos não serão considerados.
Apenas os fabricantes cujos produtos tenham sido qualificados por MSF serão considerados para compras.

Garantia de qualidade relacionada com a aquisição de produtos médicos
Princípios gerais
Como organização médica, MSF distribui/utiliza regularmente produtos médicos: medicamentos, dispositivos médicos e alimentos médicos especializados aos pacientes nos programas que desenvolve em todo o mundo. MSF atribui a maior importância à qualidade destes produtos médicos utilizados ou distribuídos aos pacientes.
MSF considera firmemente que qualquer doente, onde quer que viva, tem o direito de ser tratado com produtos médicos eficazes e seguros, e que é responsabilidade legal e moral da organização garantir a qualidade dos produtos médicos utilizados e distribuídos nos seus programas.
Tal como muitos outros atores humanitários, MSF é consciente de que a qualidade dos produtos médicos nem sempre é devidamente garantida no mercado global. Para este fim, MSF criou os seus próprios centros de abastecimento internacional, que são responsáveis pela compra, armazenamento e expedição de produtos para que MSF desempenhe as suas missões: MSF Logistique em França, MSF Supply na Bélgica, e Amsterdam Procurement Unit na Holanda. O seu objetivo é duplo:
- Operacional: para adquirir e fornecer produtos médicos e não médicos a projetos MSF em tempo útil.
- Qualitativa: para assegurar a conformidade dos produtos com os requisitos técnicos de MSF seguindo as normas internacionais e para controlar a sua qualidade.
Política de compras de MSF
O princípio principal da política de aquisições de MSF é que, como norma padrão, MSF adquire internacionalmente através dos seus centros de abastecimento os produtos médicos aprovados através da qualificação MSF.
MSF cumpre toda a regulamentação nacional aplicável relativa aos processos de importação, tal como definida pela Autoridade Nacional Competente e em conformidade com o Memorando de Entendimento (MdE) dos países e, quando existente, com o Acordo de País Anfitrião (HCA).
Em alguns países, contudo, MSF não está autorizado a importar produtos médicos. Nesse caso, a responsabilidade legal de assegurar a qualidade dos produtos médicos recai sobre as Autoridades Reguladoras Nacionais de Medicamentos. Dentro desse quadro, MSF aplica um procedimento específico de validação de compras locais.
MSF não aceita doações em espécie de produtos médicos ou tecnologia de saúde. Em circumstâncias excepcionais, e numa base caso a caso, MSF pode considerar aceitar tais doações de acordo com os critérios e condições estabelecidos na Política de Doações em Espécie de Produtos Médicos e Tecnologia da Saúde de MSF.
Gestão de Reclamações e Não-Conformidades de Qualidade
MSF segue um Procedimento para a Gestão de Reclamações e Não Conformidades de Qualidade, e para tratar da recolha de produtos médicos, aplicável tanto a nível dos Centros de Abastecimento que conduzem aquisições internacionais como a nível de projetos.
MSF exige dos seus fornecedores um sistema de rastreabilidade e um procedimento de controle das reclamações de qualidade e de ativação de recolhas (recalls).
Farmacovigilância
As reações adversas aos medicamentos e as questões de qualidade dos medicamentos são acompanhadas de perto nos projetos de MSF.
Estas situações são investigadas atempadamente, geralmente em colaboração com o(s) fabricante(s) do(s) medicamento(s), os farmacêuticos locais e centrais de MSF e as agências reguladoras de medicamentos onde MSF trabalham (se aplicável), para determinar a causa raiz dos problemas e as acções corretivas e preventivas adequadas.
Diretriz de armazenamento de produtos médicos MSF
MSF desenvolveu directrizes internas para Boas Práticas de Armazenamento e Distribuição baseadas nas Boas Práticas de Armazenamento e Distribuição de produtos médicos da OMS, 2020. Há também formação regular prestada internamente.


Procesos de calificación de MSF para productos médicos

Proceso de calificación de MSF para alimentos para fines medicinales especiales

Proceso de calificación de MSF de dispositvos médicos y diagnósticos in vitro

Proceso de calificación de medicamentos de MSF
Procesos de calificación de MSF para productos médicos
Como muchas otras organizaciones humanitarias, MSF es consciente de que la calidad de los medicamentos y otros productos médicos no siempre está debidamente garantizada en el mercado mundial<p><a href="https://apps.who.int/iris/bitstream/handle/10665/330145/9789241517034-eng.pdf?sequence=1&isAllowed=y"><span style="font-size: 11.0pt; line-height: 107%; font-family: 'Calibri',sans-serif; mso-ascii-theme-font: minor-latin; mso-fareast-font-family: Calibri; mso-fareast-theme-font: minor-latin; mso-hansi-theme-font: minor-latin; mso-bidi-font-family: Arial; mso-bidi-theme-font: minor-bidi; mso-ansi-language: EN-US; mso-fareast-language: EN-US; mso-bidi-language: AR-SA;">Hoja de ruta para el acceso a medicamentos, vacunas y otros productos sanitarios 2019-2023, OMS </span></a></p>. El equipo de coordinación de la Oficina Internacional de Garantía de Calidad (IO QA) ha desarrollado tres esquemas de calificación para la aprobación interna de:
- medicamentos
- productos sanitarios, diagnósticos in vitro y artículos de laboratorio; y
- alimentos terapéutcos especializados.
Principios:
- La calificación es un procedimiento estandarizado de evaluación de la calidad para validar (o no) los productos médicos antes de que puedan adquirirse para su uso por parte de MSF, verificando que el producto cumple al menos las normas de calidad reconocidas internacionalmente. El proceso de calificación consiste en la evaluación del expediente del producto y del lugar de fabricación (por ejemplo, una auditoría de Buenas Prácticas de Manufactura, BPM).
- Los procedimientos de calificación de MSF se basan en la confianza mutua. Se pide al fabricante que certifique la veracidad y exactitud de la información y los documentos presentados a MSF. Los errores u omisiones pueden llevar a la descalificación del producto y/o del fabricante.
- Los esquemas de calificación de MSF no pretenden interferir con la iniciativa de precalificación de la Organización Mundial de la Salud (OMS), ni duplicar ningún trabajo existente llevado a cabo por el grupo de autoridades reconocidas como SRA (Stringent Regulatory Authority) por la OMS. Por lo tanto, cualquier producto médico precalificado por la OMS o fabricado y registrado y /en el mercado de una autoridad reconocida como SRA por la OMS es automáticamente calificado por MSF.
- MSF no es una Agencia Reguladora ni un organismo certificador. El sistema de calificación de MSF ha sido diseñado exclusivamente para MSF y las decisiones tomadas sólo son válidas para MSF. Las decisiones se toman utilizando un sistema de calificación predefinido, para garantizar la imparcialidad.

Método
Las diferentes etapas del proceso se basan en lo siguiente:
- Pre-evaluación basada en el cuestionario del producto y/o del fabricante.
- Buenas Prácticas de Manufactura (BPM): inspección del lugar de fabricación: la evaluación del cumplimiento por parte del centro de producción de las Buenas Prácticas de Manufactura (BPM) es el primer paso necesario dentro de la evaluación. Para las medicinas, sólo serán evaluados productos fabricados en una planta de fabricación que cumple con las BPM de acuerdo con la OMS. Las inspecciones de BPM conducidas por el programa de precalificación de la OMS (WHO PQ) o cuerpos de inspectores reconocidos por MSF son tomados en consideración por MSF. Para fábricas que no han sido previamente inspeccionadas y aprobadas por la OMS (WHO PQ) o un cuerpo de inspectores de una autoridad reconocida como SRA por la OMS, el Coordinador Internacional de Garantía de Calidad de MSF designará a un experto en BPM para realizar la inspección.
- Evaluación del producto: para medicinas, la evaluación se basa en el cuestionario de producto/fabricante, de acuerdo a los estándares definidos por la OMS, y basado en un cuestionario estándar común al Grupo de Farmacéuticos Interagencia (UNICEF, CICR, El Fondo Mundial, centro de compras de la OMS, FNUAP, GDF y MSF).
- Control y seguimiento activos
Procesos de calificación de MSF

Proceso de calificación de medicamentos de MSF

Proceso de calificación de MSF de dispositvos médicos y diagnósticos in vitro

Proceso de calificación de MSF para alimentos para fines medicinales especiales
Si la evaluación es satisfactoria, se emite una "hoja de especificaciones del producto" (del inglés “Product Specifications Sheet, PSS) que resume las características del producto aprobadas por MSF, y que se utiliza como referencia para la adquisición.
La calificación de MSF es un procedimiento continuo y los productos aprobados se supervisan a intervalos regulares. Las actividades de seguimiento se centran en la reevaluación del cumplimiento de las Buenas Prácticas de Manufactura (BPM) del centro de producción y en la actualización de la información y los datos facilitados en la evaluación del producto.
Expresión de interés
Los fabricantes y proveedores de productos médicos, medicamentos, vacunas, productos terapéuticos especializados, reactivos y equipos de laboratorio, y material y equipos médicos son bienvenidos a expresar su interés en convertirse en proveedores validados por MSF, enviando un correo electrónico al asistente de los coordinadores de garantía de calidad a [email protected]
No se tendrán en cuenta los productos que no figuren en la lista de medicamentos de MSF, la lista de alimentos terapéuticos especializados de MSF o la lista de productos sanitarios de MSF.
Sólo se tendrán en cuenta para la compra los fabricantes cuyos productos hayan sido calificados por MSF.
Article 1 of the United Nations Convention on the Rights of the Child, adopted and opened for signature, ratification and accession by General Assembly resolution 44/25 of 20 November 1989, entry into force 2 September 1990, in accordance with article 1: “For the purposes of the present Convention, a child means every human being below the age of eighteen years unless under the law applicable to the child, majority is attained earlier.


Amid hunger, people are “lucky to be alive” in northwest Nigeria

Processus de qualification MSF pour les produits médicaux

How we deliver medical humanitarian assistance
Everywhere we work, the circumstances are unique. Nonetheless, our programmes generally follow a common set of practices designed to make sure our resources and expertise are used to maximum effect.